Startup koji je prvi uspješno obavio presađivanje svinjskog bubrega u čovjeka najavio nove poduhvate
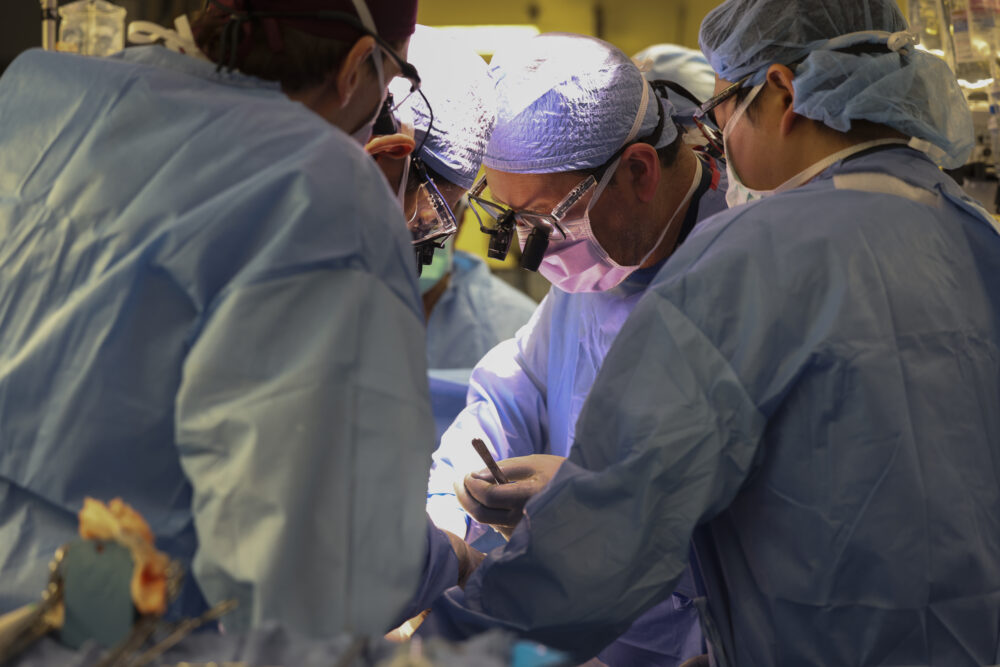
Biotech startup eGenesis razvio je genetski modificirani bubreg koji je prošlog tjedna uspješno presađen u čovjeka. Izvršni direktor tvrtke kaže kako je ovo tek početak. Priprema se presađivanje – srca i jetre
Kirurzi Opće bolnice u Massachusettsu prošlog tjedna su objavili kako je po prvi put ljudskom pacijentu presađen bubreg svinje. Ovaj znanstveni iskorak pruža nadu desecima ljudi koji svaki dan umiru čekajući transplantaciju organa, rekao je direktor bolnice za transplantacije Joren Masden na konferenciji za medije. “San istraživača transplantacija je korištenje svinjskih organa kako bi se riješio problem nestašice,” dodao je.
Naravno, to nije baš jednostavno. Ovaj bubreg razvio je startup iz Massachusettsa eGenesis koji već gotovo deset godina radi ne genetskom modificiranju svinjskih organa kako bi ih se moglo sigurno presaditi u ljude. Ipak, izvršni direktor startupa Mike Curtis za Forbes kaže kako je prošlotjedno postignuće tek početak. Njegova tvrtka, koja je dosad od investitora prikupila 291 milijun dolara, želi svoju tehnologiju modificiranja gena za transplantacije bubrega, jetre i srca u sljedeće dvije godine dovesti u fazu kliničkih testiranja, čime bi ona postala novi igrač na tržištu koje, prema procjenama Grand View Researcha, vrijedi oko 15 milijardi dolara.
“Pokazali smo da zaista imamo nešto što može pomoći pacijentima,” kaže on. “Za mene se sve svodi na dolazak nove ere znanosti i pružanja pomoći ljudima koji imaju vrlo malo opcija za liječenje.”
U SAD-u trenutno na organe čeka preko stotinu tisuća ljudi, ali u godini dana će manje od polovice njih dobiti presađeni organ zbog nedostatka donatora. Desetljećima znanstvenici vjeruju kako bi životinjski organi nekim pacijentima mogli pomoći, čak i samo kao način da ih dovoljno dugo održe na životu kako bi mogli dobiti ljudski organ. Svinje su idealni kandidati jer odrastaju brzo, a njihovi organi imaju sličnu veličinu i funkcionalnosti kao i ljudski.
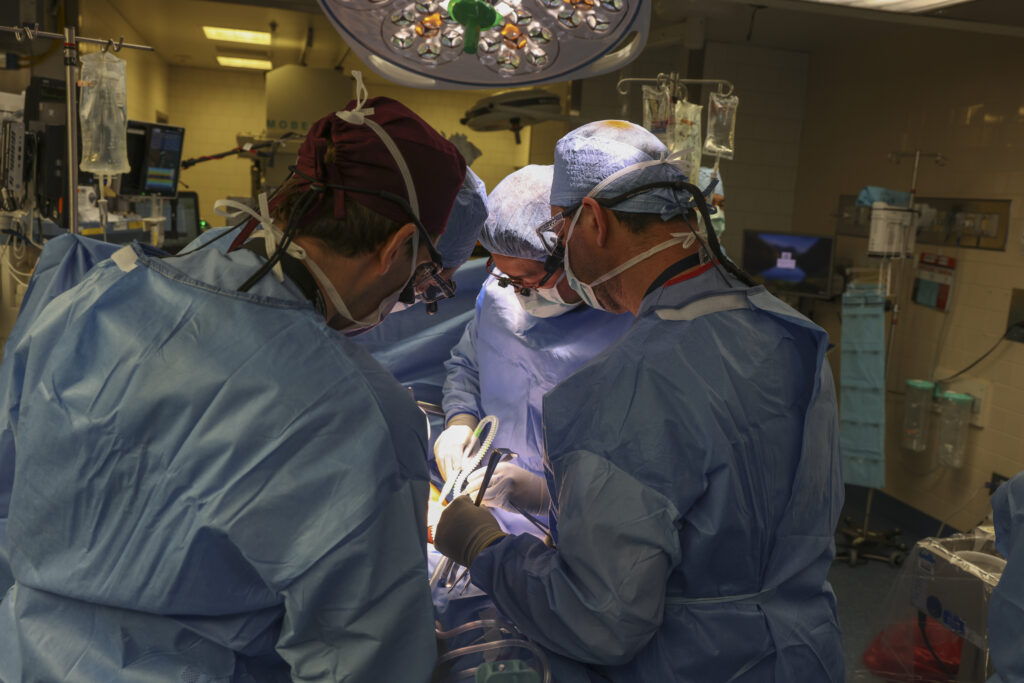
U ovom slučaju, pacijent je bio 62-godišnji muškarac čiji su ranije presađeni bubrezi otkazali, a procedura je dobila svjetlo programa “proširenog pristupa” američke Administracije za hranu i lijekove (FDA). Taj program omogućava pacijentima s po život opasnim bolestima da iskušaju eksperimentalne lijekove ili procedure. Ova operacija uslijedila je nakon nekoliko eksperimenata, kao i dvije druge operacije u kojima su živim pacijentima presađena genetski modificirana srca.
Jamil Azzi, kirurg u bolnici Brigham koji nije sudjelovao u operaciji od četvrtka, pohvalio je operaciju. “To je velika prekretnica do koje se dolazilo desetljećima,” rekao je on za Forbes, ali ipak upozorio kako je potrebno još mnogo podataka prije nego ovakva vrsta operacije postane rutinska. Ključno pitanje je koliko dugo donirani svinjski bubreg može funkcionirati u ljudskom pacijentu. “Ako otkaže nakon dva ili tri mjeseca, to znači da daleko zaostajemo,” rekao je. Prošle godine svinjska srca presađena su u dva pacijenta. Srca je razvila tvrtka Revivicor, podružnica United Therapeuticsa, a oba pacijenta preminuli su nekoliko tjedana nakon operacije, iako nije jasno zašto.
Jedan od najvećih izazova pri transplantacijama životinjskih organa u ljude je osiguravanje da tijelo pacijenta odmah ne odbije organ. To je već problem s bubrezima koje doniraju ljudi, a skeptici kažu kako velike razlike između svinja i ljudi ovakve vrste presađivanja čine nemogućima. Tu na scenu stupa modificiranje gena. Za prošlotjednu operaciju, objašnjava Curtis, važno je bilo genetski modificirati bubreg svinje sa sedam različitih ljudskih gena, ukloniti tri svinjska gena i 59 dodatnih dijelova DNK. Te promjene osiguravaju da bubreg neće napasti imunološki sustav pacijenta, iako su imunosupresivni lijekovi potrebni jednako kao i kod presađivanja ljudskih organa.
Ove promjene učinjene su na jednoj svinjskoj stanici, koja je potom inkorporirana u embrij i klonirana. Klonirani embriji potom su ugrađeni u ženku svinje, a njeni praščići imali su potrebne genetske promjene.
Toliko promjena, kaže Curtis, povećava rizik od toga da će se nenamjerno promijeniti drugi dijelovi životinjskog genoma. Ipak, u posljednjih nekoliko godina, napretci u sekvencioniranju genoma omogućili su detekciju takvih promjena. Tvrtka je u ovom konkretnom slučaju uspjela utvrditi da su te promjene bile minimalne i da neće utjecati na ishod.
U radu objavljenom prošle jeseni u časopisu Nature, tvrtka je govorila o slučajevima gdje su majmuni kojima su presađeni svinjski bubrezi preživjeli preko godinu dana – u jednom slučaju i preko dvije godine. Uz te podatke, kao i ovogodišnje uspješno presađivanje bubrega, Curtis kaže kako eGenesis napreduje prema tome da može službeno predati prijavu FDA-ju i krenuti u klinička testiranja već 2025. godine. Još uvijek nisu stigli do te točke: Curtis kaže kako agencija još uvijek želi dobiti više podataka o primatima prije nego tvrtci da zeleno svjetlo. Iako je potrebno više podataka, Azzi kaže kako je ono što je dosad pokazano “dobar indikator” da je tvrtka na pravom putu.
Ono što će morati učiniti da dođu na sljedeću razinu, kaže Curtis, jest doći do točke gdje će se njihove svinje moći uzgajati s organima spremnima za donaciju, umjesto da postoji potreba za kloniranjem i implantacijom. George Church, suosnivač eGenesisa i istraživač genetike u medicinskoj školi na Harvardu, za Forbes kaže kako bi im to moglo omogućiti da nekoliko organa za pacijente može doći od jedne svinje.
“Krajnja vizija je stvaranje organa u svinjama koji ne zahtijevaju imunosupresivne lijekove.”
Mike Curtis, CEO, eGenesis
Nešto bliže ostvarenju, kaže Curtis, su programi tvrtke za modificiranje svinjske jetre i srca za transplantaciju u ljudske pacijente, u kojma koriste slične procese kao i kod bubrega. U siječnju je tvrtka objavila uspješnu operaciju pri kojoj su genetski modificiranu svinjsku jetru izvana povezali s pacijentom kojemu je dijagnosticirana moždana smrt. Ova procedura mogla bi pomoći pacijentima kojima je otkazala jetra preživjeti ključnih nekoliko dana kako bi mogli dobiti ljudski organ.
Zahvaljujući ovom uspjehu, Curtis kaže kako kompanija planira podnijeti prijavu FDA-ju za genetski modificiranu jetru, a s kliničkim testiranjima planiraju započeti krajem godine. Tvrtka s vremenom želi da se njihove modificirane jetre u potpunosti presađuju u žive pacijente.
Trajna transplantacija cilj je eGenesisa što se tiče bubrega i jetre, ali kod programa za srce, Curtis kaže kako tvrtka uglavnom razmatra pedijatrijske pacijente za koje bi svinjsko srce moglo biti prijelazno rješenje dok ne dobiju ljudski organ. Trenutno, kaže on, preko 50 posto djece kojima je potrebno novo srce premine dok čeka na operaciju. Tvrtka je zasad zabilježila da pavijani s genetski modificiranim srcem prežive preko 200 dana, a Curtis kaže kako se nada da bi to moglo “dovesti do napretka u polju pedijatrijskog presađivanja srca, ili kasnije ove ili početkom sljedeće godine.”
Dugoročne ambicije tvrtke još su veće. “Krajnja vizija je stvaranje organa u svinjama koji ne zahtijevaju imunosupresivne lijekove,” kaže Curtis. To bi moglo značiti da pacijenti kojima su presađeni organi ne moraju uzimati lijekove koji usporavaju imunološki sustav i tako sprječavaju odbijanje organa. Iako ih to drži na životu, također povećava rizik od infekcije i raka. “Znamo da će to zahtijevati dodatni inženjering, ali trebat će nam ljudski podaci kako bismo mogli vidjeti točno kako će on točno morati izgledati,” dodaje.
Istraživač i suosnivač eGenesisa George Church kaže kako potencijal genetskog inženjeringa znači kako će tvrtka možda jednog dana moći stvarti “poboljšane organe.” Na primjer, kaže on, možda je moguće modificirati svinjski genom za stvaranje “organa otpornih na neke patogene”, a možda čak i organa koji sporije stare. Kao dokaz tog koncepta on navodi istraživanje u njegovom laboratoriju na Harvardu čiji recenzirani rezultati su objavljeni u časopisu Nature, a tijekom kojega je zbog jedne jednostavne genetske promjene jedna vrsta bakterija postala otporna na sve poznate viruse. “Sada to želimo učiniti i na svinjama,” kaže on.
U bližoj budućnosti, tvrtka će morati povećati obujam rada, što će zahtijevati i više kapitala, kaže Curtis. Oni zasad imaju dovoljno sredstava do kraja 2026. godine, a već su u procesu prikupljanja novih, dodaje. On se nada kako uspješna operacija potencijalnim investitorima može služiti kao znak da je kompanija na pravom putu.
“Ova prva transplantacija bubrega u živog pacijenta potvrđuje naš cijeli pristup,” kaže on. “Dopustit će nam ne samo da krenemo s bubrezima, već paralelno i sa srcem i jetrom.”
Autor originalnog članka: Alex Knapp, Forbes
Link: The Startup Behind The First Pig-Human Kidney Transplant Is Targeting Hearts And Livers Next
(Prevela: Nataša Belančić)








